Mikroplasty a nanoplasty v životním prostředí
MICROPLASTICS AND NANOPLASTICS IN THE ENVIRONMENT
Marek Nechvátal1,2, Karel Klouda1,2
1Výzkumný ústav bezpečnosti práce, v. v. i., nechvatal@vubp-praha.cz, klouda@vubp-praha.cz
2Vysoká škola báňská – Technická univerzita Ostrava, Fakulta bezpečnostního inženýrství
Abstrakt
Článek souhrnně zpracovává poznatky o vlivu mikro a nanoplastů na složky životního prostředí. Uvádí nejčastější zdroje mikro- a nanoplastů, transformaci a způsoby jejich likvidace a recyklace. Pozornost je věnována komplexnímu souboru hlavních určujících faktorů toxicity plastových částic v příslušných složkách prostředí, novým zdrojům (odpady z respirátorů, roušek a masek), interakci s volně žijícími živočichy a kontaminantům, které se mohou uvolňovat z takových ochranných prostředků a které mají potenciál vyvolat ekotoxikologické škody.
Klíčová slova: mikroplasty, nanoplasty, nanočástice, nanotextilie, respirátory, toxicita, životní prostředí, plastový odpad
Abstract
The article summarizes the knowledge about the influence of micro and nanoplastics on environmental components. Lists the most common sources of micro and nanoplastics, transformation and methods of their disposal and recycling. Attention is paid to a comprehensive set of main determinants of plastic particle toxicity in relevant environmental compartments, new sources (respirator wastes, drapes and masks), interaction with wildlife and contaminants that may be released from such protective devices and which have the potential to cause ecotoxicological damage.
Keywords: microplastics, nanoplastics, nanoparticles, nanotextiles, respirators, toxicity, environment, plastic waste
Přijat k publikování / Received for publication 27. 10. 2021
Úvod
Plasty jsou moderním produktem, který využívá naše společnost ve všech odvětvích, včetně zdravotnictví a potravinářského průmyslu. Vzhledem k tomu, že průmyslová výroba plastů začala již ve 40. letech 20. století, objemy vyrobených plastů překonaly téměř jakýkoli jiný materiál [1]. Nicméně ty samé vlastnosti (např. tvarovatelnost, pružnost, odolnost vůči vodě, korozi, chemickým látkám a biologickým činitelům), které činí plasty vysoce žádanými, jsou také těmi, které životní prostředí (ŽP) ohrožují. Pouze 9 % veškerého vyrobeného plastu bylo recyklováno. Většina plastového odpadu končí na skládkách a nakonec v ŽP [2], [3].
Většina plastů v prostředí chemicky nedegraduje. Místo toho se pomalu fragmentují na menší částice, označované jako mikroplasty a nanoplasty. Mikroplasty jsou obvykle úlomky s velikostí pod 5 mm, nanoplasty s velikostí mezi 1 a 100 nm. Tyto částice, ať už ve formě větších, nebo menších rozměrů, jsou vysoce škodlivé pro ekosystémy, biotu a ŽP, ale také pro hospodářství a lidské zdraví [2], [3], [4], [5].
Vznik mikro a nanoplastů a jejich zdroje
V současnosti jsou mikroplasty a nanoplasty v ŽP všudypřítomné. Lze je nalézt ve vnitřním i venkovním vzduchu, ve vodě a sedimentech a v suchozemských a vodních organizmech. Jejich hlavní zdroje se liší, ale většinou pocházejí z plastů na jedno použití, textilu a kosmetiky, rybářského vybavení, barev, pneumatik či městského prachu [3].
Mikroplasty se podle svého původu a způsobu vzniku dělí do dvou skupin - na primární a sekundární. Primární mikroplasty jsou ty, které se do ŽP dostaly v podobě malých plastových částic, např. jako součást průmyslových brusiv, vrtných kapalin, kosmetických výrobků (např. zubní pasty, peeling), čisticích prostředků či opracováváním plastových materiálů [6, 7], sjížděním pneumatik a praním plastového oblečení [8].
Sekundární mikroplasty vznikají rozpadem větších plastových výrobků, které se dostaly do ŽP. Nejčastějším zdrojem sekundárních mikroplastů je plastový odpad (plastové lahve, tašky, jednorázové plastové obaly na potraviny, plastové textilie apod.), a to jak skládkovaný, tak odložený do ŽP mimo skládky, vyřazené rybářské vybavení nebo nátěry na bázi syntetických polymerů (např. lodní, silniční či fasádní barvy) [6, 7].
Podobně jako mikroplasty mohou být též nanoplasty uvolňovány do prostředí přímo nebo v důsledku fragmentace větších částic. Zcela analogicky proto mohou být také nanoplasty klasifikovány jako primární nebo sekundární. Primární nanoplasty zahrnují nanomateriály nacházející se cíleně ve výrobcích, jako jsou barvy, lepidla a elektronika, nebo vznikající při různých výrobních činnostech. Také různé činnosti, jako je tepelné řezání polystyrenu (PS) nebo polyvinylchloridu (PVC), stejně jako stále oblíbenější a dostupnější 3D tisk, který vede k uvolňování částic malých až 11,5 nm, mohou vést k uvolňování nano- a mikroplastů do ŽP. Sekundární nanoplasty vznikají fragmentací větších plastových částic, jako jsou mikroplasty. Přesný mechanizmus, kterým k tomu dochází, je však stále nejasný [2].
Při výrobě konečných produktů (finálních výrobků, např. respirátorů, roušek, masek) může docházet k emisi nanočástic, zejména pokud nejsou přísně kontrolovány pracovní postupy. Mohou nastat dva různé typy emisí [16]:
- přímé emise (např. nefunkční nebo nesprávně navrženou filtroventilací, příp. náhodným únikem),
- nepřímé emise (např. nevhodným zpracováním odpadu).
Během fáze výroby konečných produktů (finálních výrobků) se emise zvyšují při procesech strukturální modifikace materiálu obsahujícího nanočástice, jako je stříhání, řezání, broušení apod. nebo postupy, které vyžadují vysokou energii a teplotu pro výrobu úpravy tvaru [17].
Likvidace a recyklace plastů jako zdroj nano- a mikroplastů
Plasty jsou velmi stabilní materiály. Biologicky jsou obtížně rozložitelné, a proto se významně podílejí na znečistění ŽP na globální úrovni.
Plastový odpad je pro ŽP významným zdrojem nano- a mikroplastů. Proto má na úroveň znečistění ŽP nano- a mikroplasty vliv jeho odstraňování, případně další zpracování (recyklace).
Plasty lze skládkovat, spalovat nebo recyklovat. Na skládce obvykle končí většina odpadů z plastu [9]. V závislosti na odolnosti vůči degradaci a systémech řízení skládek mohou nebo nemusí uvolňovat mikro- a nanočástice plastu do ŽP [10]. Při spalování plastů jsou emitovány částice popela, přičemž nanočástice mohou být jejich součástí [9]. Díky vysoké účinnosti filtrů ve spalovnách (vyšší než 99,6 %) jsou přímé emise těchto částic do ovzduší velmi nízké [11]. K emisím mikro- a nanočástic může dojít i v průběhu recyklačního procesu plastu v závislosti na odolnosti jeho materiálu [11].
Osud plastů v životním prostředí
Jakmile se plasty dostanou do ŽP, mohou být degradovány abiotickými a/nebo biotickými procesy [2].
Modifikované plastové materiály jsou téměř výlučně těmi, které se dostanou do ŽP, např. z výrobků. Transformace přímo ovlivňují toxicitu mikro- a nanočástic a dopad na živé organismy. K transformacím může dojít v jakékoli fázi životního cyklu plastu, od fáze výroby až po skládkování. Transformací mohou vznikat mikro- a nanočástice plastu, které se od původních liší fyzikálními nebo chemickými vlastnostmi [12]:
- fotochemická transformace - v závislosti na vlnové délce dopadajícího záření, penetrační kapacitě a fotocitlivosti plastu může být excitace a jejich následná transformace větší nebo menší;
- oxidace a redukce - tyto procesy mohou nastat, když je reakce termodynamicky příznivá, takže závisí na médiu a podmínkách obklopujících plastový materiál (pH, přítomnost oxidačních a redukčních činidel, nebo stabilizátorů);
- rozpouštění a srážení - může dojít k rozpuštění iontů nebo molekul rozpustných ve vodě, ale také k následnému srážení nové pevné látky, která obsahuje kromě nanočástic i další ligandy přirozeně přítomné ve vodě;
- adsorpce a desorpce - adsorpce na pevné látky může probíhat prostřednictvím Van der Waalsových sil, elektrostatických interakcí nebo chemických vazeb, zatímco změny v rovnováze mezi produkty způsobují desorpci;
- spalování - vysokoteplotní procesy, jako je spalování, vedou k reakcím, které mohou chemicky modifikovat mikro- a nanočástice plastu;
- biotransformace - zahrnuje všechny procesy uvedené výše (kromě spalování), pokud jsou zprostředkovány biologickými činiteli;
- otěr - při běžné manipulaci s některými plasty může dojít k uvolnění mikro- a nanočástic obsažených v jejich struktuře, např. polyuretanové nátěry mohou uvolňovat nanočástice po určité době.
Abiotické cesty degradace lze rozdělit na dva odlišné typy procesů, které závisejí na typu polymerního řetězce. Záleží na tom, zda polymer sestává pouze z C-C vazeb, jako je tomu v případě PS, PVC, polypropylenu (PP) a polyetylenu (PE), nebo zda jsou v řetězci přítomny heteroatomy, jako např. polyetylentereftalát (PET) a polyuretan (PU). V prvním případě je proces zahájen náhodným fotolytickým štěpením vazby C-H, zatímco v polymerních materiálech obsahujících heteroatomy je obvykle počátečním krokem hydrolýza [2].
Složitost degradačních cest je ovlivněna dalšími faktory, jako je hustota polymerů, které se mohou lišit v důsledku jevů, jako je tvorba biofilmu a agregace [2].
Biologický mechanizmus degradace plastů se obvykle iniciuje mimo buňky v důsledku enzymatické aktivity. To má za následek štěpení hlavního polymerního řetězce hydrolytickými cestami bez ohledu na médium. Nakonec ve vodě rozpustné oligomery degradují na monomery, což nakonec vede k mineralizaci. Přesto se předexpozice UV záření jeví jako klíčový faktor ovlivňující rychlost biodegradace, a to jak v půdě, tak ve vodním prostředí [2].
Plasty jsou v podstatě biochemicky inertní. Přísady v nich však často mají nízkou molekulovou hmotnost a nejsou chemicky vázány na polymery. Mohou tak vyvolávat biochemické efekty. Migrovat mohou i zbytkové monomery, které se nacházejí v polymerech v důsledku neúplných polymeračních reakcí daleko od matrice, stejně jako rozpouštědla a jiné organické polutanty adsorbované plasty z okolního prostředí. Tyto látky jsou pak schopny se vyluhovat z plastových materiálů, a protože většina z nich je často lipofilní, mají inherentní afinitu k buněčným membránám. Mohou vstupovat přes membrány do buněk a poté se aktivně účastnit biochemických reakcí. Např. polyvinylchlorid (PVC), polystyren (PS) a polykarbonát (PC) uvolňují toxické monomery spojené se vznikem reprodukčních abnormalit, stejně jako s rakovinou u bezobratlých, hlodavců a lidí [2].
Vliv nanočástic na ŽP závisí především na jejich fyzikálně-chemických vlastnostech, ekotoxicitě, transformačních procesech a způsobech emise [13]. Inherentní potenciální toxicita je zásadně podmíněna jejich schopností zasáhnout různé složky prostředí (půdu, vodu, vzduch). Tento dopad přímo souvisí s množstvím uvolněným do biosféry. Proto jsou rizika spojená s používáním nanomateriálů určována všemi procesy, které řídí jejich uvolňování do ŽP, transportem a transformacemi, které mohou nastat, jakmile jsou uvolněny [14]. Hodnocení a kvantifikace množství uvolněných nanočástic vyžaduje důkladný výzkum celého jeho životního cyklu [9], počínaje výrobními procesy nanomateriálů a konče postupy recyklace a likvidace, s přihlédnutím k tomu, jakým způsobem jsou zabudovány do konečných produktů a jaké je jejich následné využití [15].
Vznik nano- a mikroplastů v souvislosti s pandemií
K emisím nanočástic může dojít i při nošení a používání výrobků z nanomateriálů (např. respirátorů, roušek, masek). Zatímco množství nanočástic uvolňovaných do ŽP při standardním používání je omezené, známé a měřitelné, lze toto množství pouze odhadnout, pokud jde o uvolnění nanočástic způsobené poškozením či nestandardním používáním produktů. V závislosti na typu produktu a jeho vlastnostech se emise budou lišit [18]. Z kapalných částí produktu se při použití rychle uvolní téměř celý obsah nanočástic [19]. Z pevných částí produktu se však obsažené nanočástice uvolňují postupně během používání produktu (např. otěrem a třením) [20]. Nakonec některé části mohou zůstat roky stabilní (obr. 1).
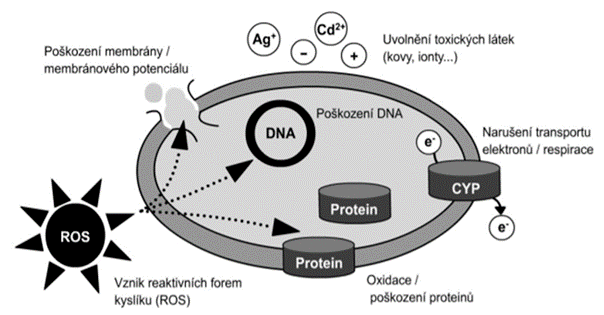
Obr. 1: Životní cyklus nanomateriálů v prostředí [21]
Respirátory, roušky, obličejové masky, šátky a další ochranné textilní prostředky
V současné době hraje klíčovou roli v mikroplastovém znečištění pandemie covid-19. Jednorázové obličejové masky apod. se používají ke zpomalení přenosové rychlosti onemocnění covid-19 z člověka na člověka. Jednorázové respirátory, roušky, masky apod. jsou v zásadě vyrobeny z PP a PE s vysokou hustotou. Mohou obsahovat další polymerní materiály, jako jsou polyestery (PES), PU, PS a polyakrylonitril (PAN). Mají tři vrstvy: vnitřní obličejová vrstva složená z měkkých vláken, střední filtrační vrstva tvořená taveninou a vnější vrstva z netkaných vláken, voděodolná a obvykle barevná [22], [23]. Tavený filtr je hlavní filtrační vrstvou masky spojený s konvenční výrobou mikro- a nanovláken, kde je roztavený polymer vytlačován malými tryskami s vysokou rychlostí foukání plynu - základní princip výroby masky na obličej pomocí elektrostatického zvlákňování.
Jakmile se dostanou do ŽP, respirátory, roušky, masky na jedno použití projdou fragmentací fyzikálně-chemickými (např. UV záření, vítr, proudy) a biochemickými (enzymatická aktivita) procesy a rozpadnou se na velké množství malých částic, jako jsou mikro- a nanoplasty (o velikosti <5 mm a <1 um, <100 nm). Jednorázové respirátory, roušky, masky apod. také obsahují aditiva pro zlepšení některých vlastností, jako jsou antivirové a antibakteriální bariéry, barviva aj. Spolu s uvolňováním mikroplastů a nanoplastů se budou uvolňovat potenciálně nebezpečné chemikálie (aditiva) [11].
Obraz o množství uvolněných mikrovláken z chirurgických obličejových masek v mořské vodě za spolupůsobení UV záření poskytl pokus, kdy byla maska podrobena 180 hdinám ozáření ultrafialovým světlem a intenzivnímu míchání s mořskou vodou a mohla uvolnit až 173 000 vláken denně [11].
Na základě studií a s ohledem na to, že miliony jednorázových respirátorů, roušek a masek se dostanou do sladkovodních toků a moří, lze předpokládat, že se z nich obrovské množství mikrovláken uvolňuje denně [11]. Při nejnižší mechanické zátěži (tj. 1,6 kJ/l, srovnatelné s energií větru ve středně silném větrném dni nebo pomalém přílivovém pohybu se odhaduje, že jediná maska s trojitou vrstvou uvolní 2,6 ± 0,7 x 10 3 mikrovláken (> 100 µm) s průměrnou délkou 1,7 ± 0,4 mm. Podle údajů průtokové cytometrie je průměrné množství mikro/nanoplastů (0,1–100 µm) generované z jednorázových obličejových masek 2,1 ± 1,4 × 10 10 položek/maska [16].
Mikroplastická vlákna jsou již v některých prostředích realitou s vysokou dominancí, např. u hladin některých řek a moří, takže úniky nebo úmyslné odhazování jednorázových masek během pandemie covid-19 celosvětově rozšíří kontaminaci plastovými mikrovlákny. V pobřežním sedimentu bylo například pozorováno až 102,4 vláken/kg (75% zastoupeno PP a PE, včetně syntetických netkaných materiálů) nashromážděných v řece Magdalena v Kolumbii. V řece Saigon ve Vietnamu koncentrace syntetických mikrovláken dosáhla až 519 000 částic/m3 [11].
Požití a následné účinky mikrovláken (zejména PP, PE a PES, což jsou také nejběžnější polymery jednorázových obličejových respirátorů, roušek a masek) byly hlášeny u několika vodních organizmů jako filtrátoři - krabi (Carcinus maenas, Eremita analoga), drobní korýši (Hyalella Azteca, Gammarus fossarum, Daphnia magna), mlži (Mytillus edulis, Corbicula fluminea), sasanky (Aiptasia pallida) a ryby (Danio rerio) jako všežravci; kroužkovci (Tubidex tubidex) jako rozkladači. Organizmy žijící na souši rovněž dokázaly přijímat mikrovlákna jako např. půdní rozkladači, kroužkovci (Lumbricus terrestris) a plži (Achatina fulica). Požití mikrovláken (i když v koncentracích relativně vyšších než jsou ty, s nimiž se setkáváme v reálných podmínkách) často vyvolává změny chování, snižuje příjem potravy, snižuje růst/tělesnou hmotnost (zejména u korýšů), zvyšuje deformity/poškození (u ryb), snižuje reprodukční schopnosti, produkci vajíček a embryonální vývoj (u krabů), indukuje zánětlivé procesy (u sasanky), oxidační stres (u kroužkovců). Nepříznivé účinky mikroplastů v živých organizmech často souvisí s tvorbou reaktivních forem kyslíku (ROS) a následným oxidačním stresem. Ve srovnání s tvarem jiných částic (např. kulovitým) vláknité částice mají obecně vyšší ekotoxikologické účinky, zvláště když jsou taková mikrovlákna zvětralá (např. UV zářením). Plasty obsahují nespočet aditiv používaných k probarvení (např. barviva vyrobená z organických sloučenin, anorganické nebo organické pigmenty) nebo zlepšení jejich fyzikálně-chemických vlastností (např. antioxidanty), z nichž některé mají nežádoucími účinky. Například bisphenol A používaný v polykarbonátových plastech (tj. PP, PE - součást respirátorů, roušek, masek atd.) jako stabilizátor a antioxidant, se může uvolňovat z plastů a fungovat toxicky jako endokrinní disruptor. Potvrzeno bylo uvolňování organofosfátových esterů z různých typů chirurgických (KN95, FFP2, FFP3) a opakovaně použitelných obličejových masek. Chemické látky adsorbované na mikroplasty se mohou poté vyplavovat do tělesných tkání po požití/kontaktu, což má za následek indukované změny nebo bioakumulaci. Některá ze zmíněných nebezpečí, chemické látky (kovy, povrchově aktivní látky, změkčovadla, přísady) v kombinaci s mikroplasty (vlákna), působí jako stresory a vyvolávají ekotoxikologické efekty. Kromě chemikálií z výrobků z plastů mohou mikroplasty interagovat i s kontaminanty v ŽP [11].
Interakce mikroplastů s perzistentními organickými polutanty (POPs) závisí na vlastnostech mikroplastů, kontaminantů a podmínkách prostředí, což vede k aditivním, synergickým nebo antagonistickým efektům. Použité respirátory, roušky a masky často končí v odpadních vodách nebo na skládkách, kde jsou mikrovlákna vystavena vysokým koncentracím znečištění a mikroorganizmům. Mikroplasty tak např. mohou přispět k šíření genů rezistentních na antibiotika nebo zvýšit přenos plazmidů. K uvolnění kontaminantů může dojít z respirátorů, roušek anebo masek přímo do vody a půdy vystavené povětrnostním podmínkám nebo nepřímo prostřednictvím výluhů ze zpracovatelských zařízení, ze skládek odpadů, čistíren odpadních vod (ČOV), včetně kořenových, protože většina takových zařízení nemá pokročilé systémy pro eliminaci perzistentních nebezpečných chemikálií a mikro- a nanoplastů. Například kombinovaný účinek mikroplastů a mědi (kov, který se může uvolňovat) původem z obličejových roušek zvyšuje genotoxicitu, neurotoxicitu a fyziologické účinky u ryby Prochilodus lineatus. Byly také pozorovány synergické efekty u kadmia kombinovaného s mikroplasty u kapra obecného (Cyprinus carpio), s většími účinky na biochemické a imunologické parametry než pro jednotlivé stresory. Antagonistické efekty byly popsány u ryby Danio rerio, které potvrdila nižší úmrtnost při vystavení směsi kadmia a mikroplastů [11].
Chování mikročástic a nanočástic v životním prostředí
Disperzi mikro- a nanočástic v kapalině můžeme podle definice Mezinárodní unie pro čistou a užitou chemii (International Union of Pure and Applied Chemistry, IUPAC) považovat za koloidní systém. V případě částic pod 100 nm by měla být disperze stabilní a nemělo by docházet k agregaci. V reálném prostředí ale na částice působí mnoho dalších vlivů, které agregaci budou ovlivňovat [24], [25], [26].
Ve většině případů budou nanočástice po vstupu do reálného prostředí agregovat, takže pouze část těchto látek si zachová nanoformu [24], [27], [28]. Agregace nanočástic také znamená, že ve vodním prostředí bude docházet k jejich sedimentaci, čímž se budou odstraňovat z vodního sloupce. Zároveň bude docházet k hromadění u dna, takže potenciálně ohroženou skupinou organismů budou zejména ty, které žijí u dna (tzv. bentické) [24], [29]. K adsorpci vzniklých agregátů i samotné agregaci může docházet také na povrchu i uvnitř samotných organismů. K podobným adsorpčním jevům může docházet i na rozhraní fází, např. u hladiny vody, a ke kumulaci nanoplastu v těchto místech [24], [30].
Na tvorbu agregátů působí řada biotických i abiotických faktorů; některé jejich vznik podporují, další naopak disperzi stabilizují a mohou rozrušovat agregáty již vzniklé [24], [27], [30]. Jedním z působících faktorů je salinita prostředí, která podporuje agregaci nanočástic. S tím také souvisí rozdílná stabilita nanomateriálů v mořské a sladké vodě [31], [24], [25]. Některé organické látky naopak disperzi nanomateriálů stabilizují [24], [32]. Jedná se v prvé řadě o huminové látky (huminové kyseliny a fulvokyseliny) [33], [34], dále různé proteiny, polymery a povrchově aktivní látky [28]. Ty se i cíleně přidávají do produktů, aby se zabránilo agregaci [24], [25], [35]. Všechny výše uvedené látky se běžně vyskytují v ŽP. Spousta povrchově aktivních látek se do prostředí dostává i s odpadními vodami, takže stabilizace mikro- a nanočástic v prostředí působením organických látek je pravděpodobná [24], [25]. Chování mikro- a nanočástic v prostředí bude ovlivňovat řada dalších faktorů, jejichž vliv ale není dobře prozkoumán. Je to například pH (a s ním související bod nulového náboje), teplota a proudění, které ovlivňují srážky částic [25]. Svůj vliv má i koncentrace částic, přičemž při zvyšující se koncentraci se zvyšuje i míra agregace, protože srážky částic jsou častější [36]. Důležité budou i vlastnosti samotných částic jako je velikost, tvar, hmotnost, velikost povrchu, chemické složení, náboj povrchu, rozpustnost apod. [24], [26].
Vzhledem k poměrně složitému chování nanomateriálů v prostředí se nabízí otázka, zda a jakým způsobem budou ovlivňovat další kontaminanty v prostředí [24], [26], [36], [37], [38], [39]. Velký specifický povrch nanočástic ovlivňuje distribuci, transport i biologickou dostupnost kontaminantů v prostředí [26], [37], [40]. Zejména hydrofobní látky mají tendenci se v prostředí vázat na různé částice [26]. Některé aplikace nanomateriálů navíc přímo spočívají v adsorpci kontaminantů na nanostruktury, které se cíleně dávkují do vod či půd, aby tak snížily jejich kontaminaci (fullereny, uhlíkaté nanotrubice, nanoželezo) [26]. Nabízí se i ovlivnění toxicity. Nanomateriály mohou toxické účinky ostatních látek tlumit, zároveň ale může být zvýšena jejich mobilita a usnadněn tak vstup do organizmu [24], [30].
Expozice mikroplastům a nanoplastům
Expozice je situace charakterizovaná objektivními parametry, při které je živý organizmus vystaven působení chemické látky, fyzikálnímu faktoru či biologickému agens [41]. Při posuzování expozice je třeba uvažovat následující faktory [42]:
- složka prostředí, ve které se částice nacházejí (tzv. expoziční média - voda, půda, vzduch, biomasa),
- tvar částic (primárních nebo sekundárních),
- expoziční kontext (pracovníci, uživatelé nebo spotřebitelé),
- dávka částic, které je organizmus potenciálně vystaven,
- doba expozice, tedy jak dlouhou dobu je daný organizmus vystaven působení určité dávky výše jmenovaného faktoru.
Tyto výše uvedené faktory mohou rozhodovat o tom, zda daná mikro/nanočástice pronikne do organizmu, kam bude transportována a jaký bude mít vliv na životní pochody exponovaného jedince.
Závěr
Výroba a spotřeba plastů celosvětově trvale roste. Pandemie covid-19 akcelerovala jejich spotřebu a zvýšila závislost spotřebitelů i profesionálů (zdravotníků, hasičů,…) na plastových výrobcích, jako jsou např. jednorázové plastové výrobky (např. obalové materiály – pytle, potravinové obaly pro take away, hygienické materiály, injekční sety, kanyly apod.), textilie, včetně nanotextilií, vyrobených z umělých vláken (např. jednorázové osobní ochranné pomůcky, a to nejen respirátory, masky, ale i ochranné oděvy) a celá řada dalších výrobků z plastů nebo s podílem plastů.
Jedním z potenciálně významných zdrojů úniku mikro- a nanočástic do prostředí se mohou stát nanotextilie. Jednak vzhledem k jejich rozsáhlé produkci (např. nanotextilie s novými funkcemi a vlastnostmi jako součást respirátorů, roušek a dalších ochranných pomůcek) [43] a také díky prokázanému uvolňování některých nanočástic z textilních vláken během běžného používání, např. PP a PE [44].
Kromě nanotextilií a již zmíněných zdrojů nanoplastů existuje další velké množství spotřebitelských výrobků a jiných produktů, které mohou představovat expozici pro běžnou populaci i možný zdroj kontaminace ŽP. K uvolnění z těchto výrobků pravděpodobně nedochází, pokud nanočástice zůstávají navázány v polymeru nebo matrici produktu. Situace se ale mění, pokud dojde k poškození matrice při zpracování, recyklaci nebo v případě, kdy se výrobek ocitne na konci svého životního cyklu, stává se odpadem a je buď skládkován nebo spálen [45].
O vlivu na ŽP prostředí spolurozhoduje tedy systém likvidace, příp. recyklace plastového odpadu. Osobní zodpovědný přístup (třídění odpadu) a standardizovaný systém likvidace plastového odpadu, např. ve zdravotnických zařízeních, často s infekčním potenciálem, je jednou stranou mince hospodaření s plastovým odpadem, která nepředstavuje vážnější riziko pro ŽP. Naopak neodpovědné chování jedinců (prostých osob, živnostníků), ale i podniků a společností, které se snaží plastového odpadu zbavit nelegálním způsobem z ekonomických či jiných pohnutek, je neradostným případem, který může vyústit v masivní uvolňování nano- a mikoplastů do ŽP.
Tisíce tun plastů jsou dnes diseminované po celém světě a mohou tak kontaminovat ŽP nanočásticemi, mikro- a nanovlákny a nebezpečnými chemikáliemi s potenciálem vyvolat vážné škody v ekosystému od bezobratlých až po obratlovce. Při intenzivní spotřebě plastů a špatném hospodaření s odpady z plastu dojde v budoucnu s velkou pravděpodobností k dalším ekologickým problémům.
Dedikace

©2021
Literatura
[1] FREINKEL, S. Plastic: a toxic love story. Text Publishing, 2011.
[2] PINTO DA COSTA, J.; ROCHA-SANTOS, T.; DUARTE, A. C. The Environmental Impacts of Plastics and Micro-Plastics Use, Waste and Pollution: EU and National Measures. European Union, 2020. 76 s.
[3] TOUSSAINT, Brigitte …[et al.]. Review of micro- and nanoplastic contamination in the food chain. Food Additives & Contaminants: Part A. 2019, vol. 36, no. 5, s. 639-673.
[4] SOVOVÁ, T.; KOČÍ, V. Ecotoxicology of nanomaterials. Chemické listy. 2012, roč. 106, č. 2.
[5] RUPOVÁ, M.; SKŘEHOT, P. A. Bezpečnost a ochrana zdraví při práci s nanomateriály: příručka pro zaměstnavatele. Praha: Výzkumný ústav bezpečnosti práce, 2011. ISBN 978-80-86973-86-9.
[6] DUIS, K.; COORS, A. Microplastics in the aquatic and terrestrial environment: sources (with a specific focus on personal care products), fate and effects. Environmental Sciences Europe. 2016, vol. 28, no. 1, s. 2.
[7] DA COSTA, J. P. Nanoplastics in the Environment, in Plastics and the Environment. The Royal Society of Chemistry, 2019. S. 82-105.
[8] EVROPSKÝ PARLAMENT. Mikroplasty: odkud se berou, co způsobují a jak se jich zbavit? Zpravodajství [online]. 22-11-2018 [cit. 2021-12-20]. Dostupné z: https://www.europarl.europa.eu/news/cs/headlines/society/20181116STO19217/mikroplasty-odkud-se-berou-co-zpusobuji-a-jak-se-jich-zbavit.
[9] NOWACK, B. Evaluation of environmental exposure models for engineered nanomaterials in a regulatory context. NanoImpact. 2017, vol. 8, s. 38-47.
[10] NOWACK, B. …[et al.]. Potential release scenarios for carbon nanotubes used in composites. Environment International. 2013, vol. 59, 1-11.
[11] KOIVISTO, A. J. …[et al.]. Quantitative material releases from products and articles containing manufactured nanomaterials: Towards a release library. NanoImpact. 2017, vol. 5, s. 119-132.
[12] NOWACK, B. …[et al.]. Potential scenarios for nanomaterial release and subsequent alteration in the environment. Environmental Toxicology and Chemistry. 2012, vol. 31, no. 1, s. 50-59.
[13] DONG, H. …[et al.]. Aging of zero‐valent iron‐based nanoparticles in aqueous environment and the consequent effects on their reactivity and toxicity. Water Environment Research. 2020, vol 92, no. 5, s. 646-661.
[14] RAJKOVIC, S. …[et al.]. Dynamic probabilistic material flow analysis of engineered nanomaterials in European waste treatment systems. Waste Management. 2020, vol. 113, s. 118-131.
[15] GOTTSCHALK, F.; SUN, T.; NOWACK, B. Environmental concentrations of engineered nanomaterials: review of modeling and analytical studies. Environmental Pollution. 2013, vol. 181, s. 287-300.
[16] MARTÍNEZ, G. …[et al.]. Environmental Impact of Nanoparticles’ Application as an Emerging Technology: a Review. Materials. 2021, vol. 14, no. 1, s. 166.
[17] AHIRWAR, H. …[et al.]. Materials for orthopedic bioimplants: modulating degradation and surface modification using integrated nanomaterials. Coatings. 2020, vol. 10, no. 3, s. 264.
[18] GOTTSCHALK, F.; NOWACK, B. The release of engineered nanomaterials to the environment. Journal of Environmental Monitoring. 2011, vol. 13, no. 5, s. 1145−1155.
[19] MEDHI, S. …[et al.]. An investigation on the effects of silica and copper oxide nanoparticles on rheological and fluid loss property of drilling fluids. Journal of Petroleum Exploration and Production Technology. 2020, vol. 10, no. 1, s. 91-101.
[20] VEKSHA, A. …[et al.]. Heteroatom doped carbon nanosheets from waste tires as electrode materials for electrocatalytic oxygen reduction reaction: Effect of synthesis techniques on properties and activity. Carbon. 2020, vol. 167, s. 104-113.
[21] FILIPOVÁ, Z.; KUKUTSCHOVÁ, J.; MAŠLÁŇ, M. Rizika nanomateriálů. 1. vyd. Olomouc: Univerzita Palackého, 2012. ISBN 978-80-244-3201-4.
[22] SILVA, A. L. P. …[et al.]. Risks of covid-19 face masks to wildlife: Present and future research needs. Science of The Total Environment. 2021, vol. 792, no. 148505.
[23] FADARE, O. O.; OKOFFO, E. D. Covid-19 face masks: a potential source of microplastic fibers in the environment. The Science of the Total Environment. 2020, vol. 737, no. 140279.
[24] HANDY, R. D.; OWEN, R.; VALSAMI-JONES, E. The ecotoxicology of nanoparticles and nanomaterials: current status, knowledge gaps, challenges, and future needs. Ecotoxicology. 2008, vol. 17, no. 5, s. 315-325.
[25] HANDY, R. D. …[et al.]. The ecotoxicology and chemistry of manufactured nanoparticles. Ecotoxicology. 2008, vol. 17, no. 4, s. 287-314.
[26] KLAINE, S. J. …[et al.]. Nanomaterials in the environment: behavior, fate, bioavailability, and effects. Environmental Toxicology and Chemistry: an International Journal. 2008, vol. 27, no. 9, s. 1825-1851.
[27] GRIFFITT, R. J. …[et al.]. Effects of particle composition and species on toxicity of metallic nanomaterials in aquatic organisms. Environmental Toxicology and Chemistry: an International Journal. 2008, vol. 27, no. 9, s. 1972-1978.
[28] CRANE, M. …[et al.]. Ecotoxicity test methods and environmental hazard assessment for engineered nanoparticles. Ecotoxicology. 2008, vol. 17, no. 5, s. 421- 437.
[29] MUSEE, N. …[et al.]. The effects of engineered nanoparticles on survival, reproduction, and behaviour of freshwater snail, Physa acuta (Draparnaud, 1805). Chemosphere. 2020, vol. 81, no. 10, s. 1196-1203.
[30] BAUN, A. …[et al.]. Ecotoxicity of engineered nanoparticles to aquatic invertebrates: a brief review and recommendations for future toxicity testing. Ecotoxicology. 2008, vol. 17, no. 5, s. 387-395.
[31] KAHRU, A. …[et al.]. Biotests and biosensors for ecotoxicology of metal oxide nanoparticles: a minireview. Sensors. 2008, vol. 8, no. 8, s. 5153-5170.
[32] CHAPPELL, M. A. …[et al.]. Simultaneous dispersion-dissolution behavior of concentrated silver nanoparticle suspensions in the presence of model organic solutes. Chemosphere. 2011, vol. 84, no. 8, s. 1108-1116.
[33] BAALOUSHA, M. Aggregation and disaggregation of iron oxide nanoparticles: Influence of particle concentration, pH and natural organic matter. Science of the Total Environment. 2009, vol. 407, no. 6, s. 2093-2101.
[34] LI, D. …[et al.]. Effect of soil sorption and aquatic natural organic matter on the antibacterial activity of a fullerene water suspension. Environmental Toxicology and Chemistry: an International Journal. 2008, vol. 27, no. 9, s. 1888-1894.
[35] FRANKLIN, N. M. …[et al.]. Comparative toxicity of nanoparticulate ZnO, bulk ZnO, and ZnCl2 to a freshwater microalga (Pseudokirchneriella subcapitata): the importance of particle solubility. Environmental Science & Technology. 2007, vol. 41, no. 24, s. 8484-8490.
[36] CHRISTIAN, P. …[et al.]. Nanoparticles: structure, properties, preparation and behaviour in environmental media. Ecotoxicology. 2008, vol. 17, no. 5, 326-343.
[37] NAVARRO, E. …[et al.]. Environmental behavior and ecotoxicity of engineered nanoparticles to algae, plants, and fungi. Ecotoxicology. 2008, vol. 17, no. 5, s. 372-386.
[38] FARRÉ, M. …[et al.]. Ecotoxicity and analysis of nanomaterials in the aquatic environment. Analytical and Bioanalytical Chemistry. 2009, vol. 393, no. 1, s. 81-95.
[39] BAUN, A. …[et al.]. Toxicity and bioaccumulation of xenobiotic organic compounds in the presence of aqueous suspensions of aggregates of nano-C60. Aquatic Toxicology. 2008, vol. 86, no. 3, s. 379-387.
[40] ZHANG, X. …[et al.]. Enhanced bioaccumulation of cadmium in carp in the presence of titanium dioxide nanoparticles. Chemosphere. 2007, vol. 67, no. 1, s. 160-166.
[41] RUPOVÁ, M.; SKŘEHOT, P. A. Bezpečnost a ochrana zdraví při práci s nanomateriály: příručka pro zaměstnavatele. Praha: Výzkumný ústav bezpečnosti práce, 2011. ISBN 978-80-86973-86-9.
[42] BAENZA-SQUIBAN, A.; LANONE, S. Exposure, uptake and barriers. In: HOUDY, P.; KAJMANI, M.; MARANO, E. Nanoethics and Nanotoxicology. Springer, 2011. S. 37–61.
[43] SOM, C. …[et al.]. Environmental and health effects of nanomaterials in nanotextiles and façade coatings. Environment International. 2011, vol. 37, s. 1131- 1142.
[44] GRESLER, S. …[et al.]. Nano-Textiles. NanoTrust Dossiers [online]. December 2010, no. 015en [cit. 2021-12-20]. Dostupný z: http://epub.oeaw.ac.at/ita/nanotrust-dossiers/dossier015en.pdf.
[45] SAVOLAINEN, K. …[et al.]. Risk assessment of engineered nanomaterials and nanotechnologies: a review. Toxicology. 2010, vol. 269, no. 2-3, s. 92-104.
Vzorová citace
NECHVÁTAL, Marek; KLOUDA, Karel. Mikroplasty a nanoplasty v životním prostředí. Časopis výzkumu a aplikací v profesionální bezpečnosti [online]. 2021, roč. 14, č. 4. Dostupný z: https://www.bozpinfo.cz/josra/mikroplasty-nanoplasty-v-zivotnim-prostredi. ISSN 1803-3687.
Užitečné odkazy
Provozovatel portálu
Jeruzalémská 1283/9
110 00 Praha 1


